[化学电化学常识]1、原电池、电解池、电镀池判定规律 若无外接电源,可能是原电池,然后依据原电池的形成条件分析判定,主要思路是“三看”。先看电极:两极为导体且活泼性不同;再看溶液:两极插入电解...+阅读
《化学反应原理》知识点总结 第一章:化学反应与能量变化 1、反应热与焓变:△H=H(产物)-H(反应物) 2、反应热与物质能量的关系 3、反应热与键能的关系 △H=反应物的键能总和-生成物的键能总和 4、常见的吸热、放热反应 ⑴常见的放热反应: ①活泼金属与水或酸的反应 ②酸碱中和反应 ③燃烧反应 ④多数的化合反应 ⑤铝热反应 ⑵常见的吸热反应 ①多数的分解反应 ② 2NH4Cl(s)+Ba(OH)2•8H2O(s)=BaCl2+2NH3+10H2O ③ C(s)+ H2O(g) CO+H2 ④CO2+ C 2 CO 5、反应条件与吸热、放热的关系: 反应是吸热还是放热与反应的条件没有必然的联系,而取决与反应物和产物具有的总能量(或焓)的相对大小。 6、书写热化学方程式除了遵循书写化学方程式的要求外,还应注意以下几点: ①放热反应△H为“-”,吸热反应△H为“+”,△H的单位为kJ/mol ②反应热△H与测定条件(温度、压强等)有关,因此应注意△H的测定条件;绝大多数化学反应的△H是在298K、101Pa下测定的,可不注明温度和压强。 ③热化学方程式中各物质化学式前面的系数仅表示该物质的物质的量,并不表示物质的分子或原子数,因此化学计量数可以是分数或小数。必须注明物质的聚集状态,热化学方程式是表示反应已完成的数量,所以方程式中化学式前面的计量数必须与△H相对应;当反应逆向进行时,反应热数值相等,符号相反。 7、利用盖斯定律进行简单的计算 8、电极反应的书写: 活性电极:电极本身失电子 ⑴电解:阳极:(与电源的正极相连)发生氧化反应 惰性电极:溶液中阴离子失电子 (放电顺序:I->Br->Cl->OH-) 阴极:(与电源的负极相连)发生还原反应,溶液中的阳离子得电子 (放电顺序:Ag+>Cu2+>H+) 注意问题:①书写电极反应式时,要用实际放电的离子来表示 ②电解反应的总方程式要注明“通电” ③若电极反应中的离子来自与水或其他弱电解质的电离,则总反应离子方程式中要用化学式表示 ⑵原电池:负极:负极本身失电子,M→Mn+ +ne- ① 溶液中阳离子得电子 Nm++me-→N 正极: 2H++2e-→H2↑ ②负极与电解质溶液不能直接反应:O2+4e-+2H2O→4OH- (即发生吸氧腐蚀) 书写电极反应时要注意电极产物与电解质溶液中的离子是否反应,若反应,则在电极反应中应写最终产物。 9、电解原理的应用: ⑴氯碱工业:阳极(石墨):2Cl-→Cl2+2e-( Cl2的检验:将湿润的淀粉碘化钾试纸靠近出气口,试纸变蓝,证明生成了Cl2)。 阴极:2H++2e-→H2↑(阴极产物为H2、NaOH。现象(滴入酚酞):有气泡逸出,溶液变红)。 ⑵铜的电解精炼:电极材料:粗铜做阳极,纯铜做阴极。电解质溶液:硫酸酸化的硫酸铜溶液 ⑶电镀:电极材料:镀层金属做阳极(也可用惰性电极做阳极),镀件做阴极。电解质溶液是用含有镀层金属阳离子的盐溶液。 10、化学电源 ⑴燃料电池:先写出电池总反应(类似于可燃物的燃烧); 再写正极反应(氧化剂得电子,一般是O2+4e-+2H2O→4OH-(中性、碱性溶液) O2+4e-+4H+→2H2O (酸性水溶液)。 负极反应=电池反应-正极反应(必须电子转移相等) ⑵充放电电池:放电时相当于原电池,充电时相当于电解池(原电池的负极与电源的负极相连,做阴极,原电池的正极与电源的正极相连,做阳极), 11、计算时遵循电子守恒,常用关系式:2 H2~ O2~2Cl2~2Cu~4Ag~4OH-~4 H+~4e- 12、金属腐蚀:电解阳极引起的腐蚀>原电池负极引起的腐蚀>化学腐蚀>原电池正极>电解阴极 钢铁在空气中主要发生吸氧腐蚀。负极:2Fe→ 2Fe 2++4e- 正极:O2+4e-+2H2O→4OH- 总反应:2Fe + O2+2H2O=2Fe(OH)2 第二章:化学反应的方向、限度和速度 1、反应方向的判断依据:△H-T△S0反应不能自发。该判据指出的是一定条件下,自发反应发生的可能性,不能说明实际能否发生反应(计算时注意单位的换算)课本P40T3 2、化学平衡常数: ①平衡常数的大小反映了化学反应可能进行的程度,平衡常数越大,说明反应进行的越完全。②纯固体或纯溶剂参加的反应,它们不列入平衡常数的表达式 ③平衡常数的表达式与化学方程式的书写方式有关,单位与方程式的书写形式一一对应。对于给定的化学反应,正逆反应的平衡常数互为倒数 ④化学平衡常数受温度影响,与浓度无关。温度对化学平衡的影响是通过影响平衡常数实现的。温度升高,化学平衡常数增大还是减小与反应吸放热有关。 3、平衡状态的标志:①同一物质的v正=v逆 ②各组分的物质的量、质量、含量、浓度(颜色)保持不变 ③气体的总物质的量、总压强、气体的平均分子量保持不变只适用于△vg≠0的反应④密度适用于非纯气体反应或体积可变的容器 4、惰性气体对化学平衡的影响 ⑴恒压时充入惰性气体,体积必增大,引起反应体系浓度的减小,相当于减压对平衡的影响 ⑵恒容时充入惰性气体,各组分的浓度不变,速率不变,平衡不移动 ⑶对于△vg=0的可逆反应,平衡体系中加入惰性气体,恒容、恒压下平衡都不会移动 5、⑴等效平衡:①恒温恒压,适用于所有有气体参加的可逆反应,只要使...
以下为关联文档:
高中必修二化学+你问的阴阳极应该问的是电解池的问题。在电解池中阳极发生氧化反应,阴离子向阳极移动;阴极发生还原反应,阳离子向阴极移动,这样你可以判断某一级会增加某离子的浓度 判断溶液的...
高中电化学基础笔记有哪些钢铁腐蚀: 负极:Fe — 2e → Fe2+ 正极: 2H2O + O2 + 4e → 4OH—(吸氧腐蚀) 或2H+ + 4e → H2↑(析氢腐蚀) 化学和电化腐蚀及防护方法: 腐蚀速度:电解池阳极 >; 原电池负极 >; 一...
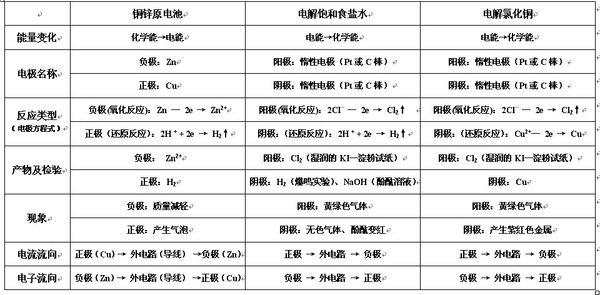
写给初中化学老师的毕业赠言语文老师、采撷一串串的梦,学校的嬉戏,回想起是那么缤纷绚丽;而成长的追逐,竟已一跃而过。世间的尘嚣喧扰,似乎沉寂,让我重新拾取记忆的落英。 数学老师、“你的一句句话就是一首...
求物理化学会考通过祝福语亲越多越好哟 3叽叽复叽叽,公鸡泡母鸡。 考试够刺激,答题靠心机。 上课听不懂,都怪老古董。 老师废话多,麻烦又啰嗦。 生是中国人,死是中国魂。 要我学英文,根本不可能。 至今思项羽,不会说英语。...
2011年给化学老师的新年祝福短信谢谢!一阵秋雨一阵凉,尊师莫忘添衣衫。当年我们太顽皮,让您着了不少急。如今只身在异乡,您的教导记心上。改日有成去见您,愿您桃李一大群。 拨动真诚的心弦,铭记成长的辛酸,成功的道路...
有什么化学方程式可以表达对教师节的祝福氢氧化钠+盐酸=氯化钠+水 祝老师家庭美满,早生贵子。化学方程式是用化学式表示化学反应的式子。化学方程式反映的是客观事实。用化学式(有机化学中有机物一般用结构简式)来表示...

高中化学知识点总结化学方程式有反应条件的无机化学部分非金属单质(F2,Cl2 , O2 , S, N2 , P , C , Si)1.氧化性:F2 + H2 === 2HF 2F2 +2H2O===4HF+O2 Cl2 +2FeCl2 ===2FeCl32Cl2+2NaBr===2NaCl+Br2Cl2 +2NaI ===2NaCl+I...
高考重点化学反应方程式1,常见气体的制取和检验 ⑴氧气 制取原理——含氧化合物自身分解 制取方程式——2KClO3 2KCl+3O2↑ 装置——略微向下倾斜的大试管,加热 检验——带火星木条,复燃 收集——排水...
高考化学考哪些知识点上海高考化学考点 1 概念的辨析(类似有机物与无机物的区分,电解质的区分) 2同位素的相对原子质量与元素平均相对原子质量 3 微粒中质子,中子数,电子数的求算 4同位素形成分子种类...